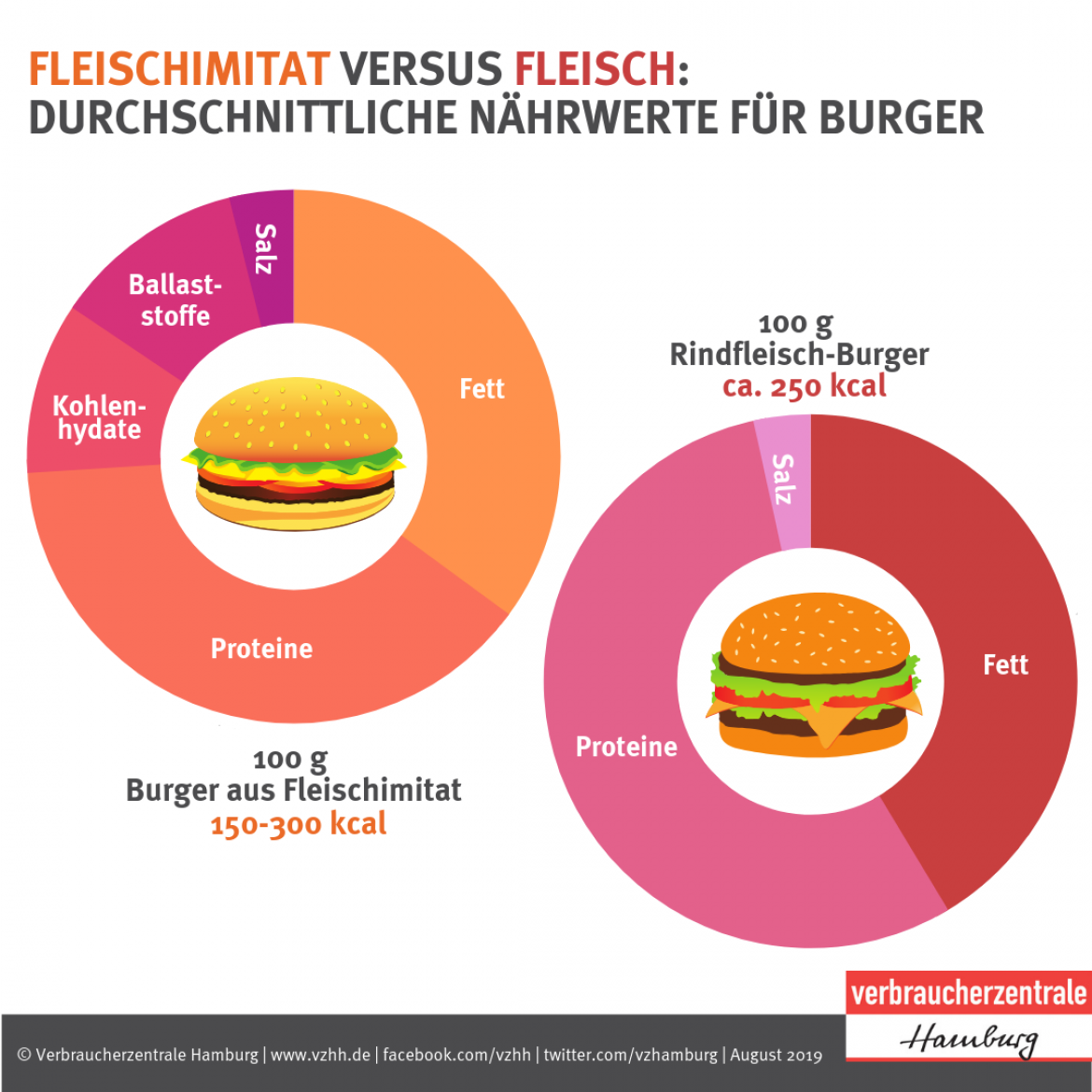
Los reactivos limitantes son ingredientes dentro de una reacción química que limitan la cantidad de producto elaborado durante una reacción química. Dentro de una reacción química, el elemento o compuesto que se agota o se consume primero es el reactivo limitante. Los reactivos limitantes también se denominan a veces reactivos limitantes.. Química Reactivo limitante. En el campo de la química conocemos con el nombre de reactivo a la sustancia que se encarga de generar una reacción química.Es una sustancia que permite mostrar la presencia de una sustancia diferente la cual por medio de una interacción, puede llegar a generar un nuevo producto.Los reactivos son entonces elementos químicos que se encargan de establecer una.

Reactivo Limitante y en Exceso (paso a paso) YouTube

Reactivo Limitante y excedente EJERCICIOS RESUELTOS YouTube

Reactivo limitante o límite y reactivo en exceso de una reacción química YouTube

Reactivo Limitante y Reactivo en Exceso en Química YouTube

05 REACTIVO LIMITE YouTube
.gif)
REACTIVOS LIMITANTES TEORIA Y EJERCICIOS RESUELTOS QUÍMICA PASO A PASO

Reactivo Limitante

problema resuelto de reactivo limitante y rendimiento YouTube

Reactivo Limitante

reactivo limitante YouTube

Reactivo Limitante Ejemplos YouTube

Reactivo Limite o Reactivo Limitante YouTube

Reactivo Limitante y en Exceso (Paso a Paso) YouTube

Reactivo LIMITANTE y en EXCESO (bien fácil) YouTube

Reactivo Limitante

QUIMICA REACTIVO LIMITANTE YouTube

Ejercicio De Reactivo Limitante
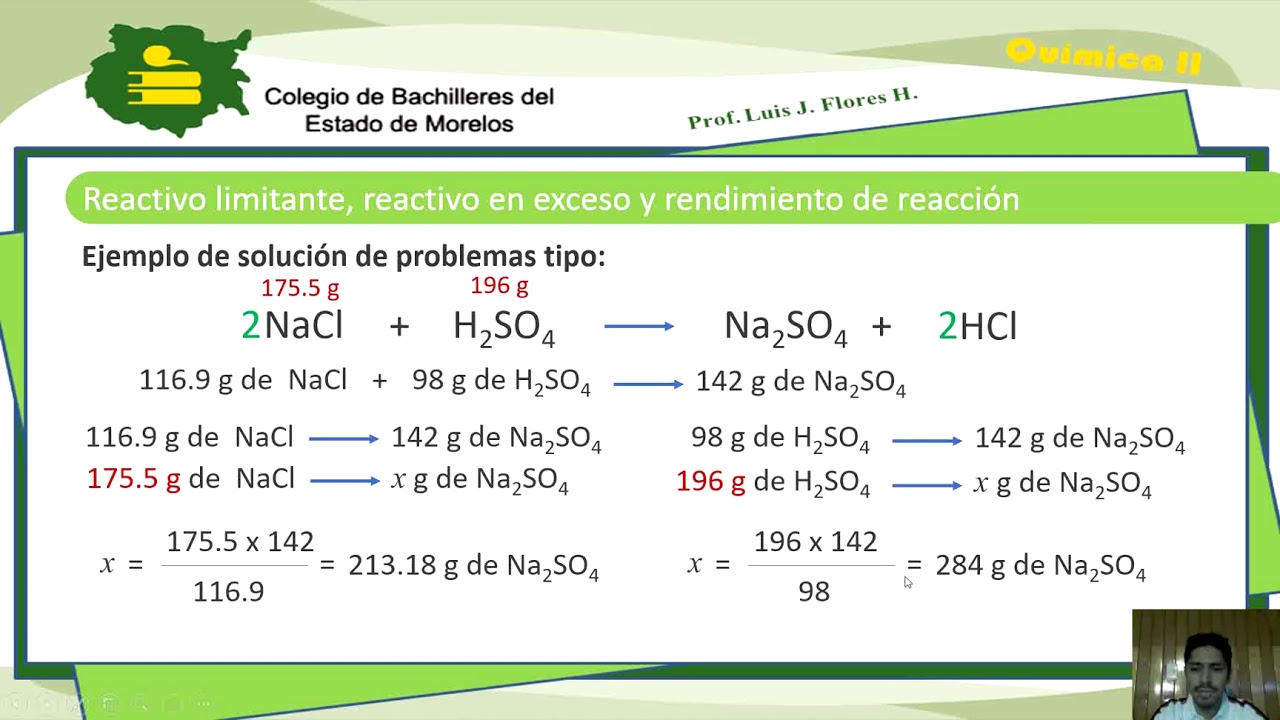
06 BACHILLERES Reactivo limitante, reactivo en exceso y rendimiento de una reacción. YouTube

¿Qué es el REACTIVO LIMITANTE o límite en química? YouTube

Reactivo Limitante
No está bien, el 3 de Oxígeno molecular que pertenece a los reactivos que mencionas tendría 6 átomos de plantearse así. La suma de átomos de oxígeno del lado de los productos, con 2 y 3 según tu resultado, tiene como resultado 5; por lo tanto no es correcto tu balanceo.. Sin embargo, en la pregunta se puede ver que solo hay 6,0 moles de HF presentes, lo que convierte al HF en el reactivo limitante. Paso 4: Identificar el reactivo que quedará; este es el exceso de reactivo. Debido a que HF es el reactivo limitante, {eq}SiO_{2} {/eq} debe ser el reactivo en exceso. Limitación de los pasos de cálculo del reactivo